Внимание! Размещенный на сайте материал имеет информационно - познавательный характер, может быть полезен студентам и учащимся при самостоятельном выполнении работ и не является конечным информационным продуктом, предоставляемым на проверку.
Задачи по курсу теплофизики
Задачи по курсу Теплофизики
Задача 1
2. Определить удельную теплоемкость cv смеси газов, содержащей 5 л водорода и 3 л гелия. Газы находятся при одинаковых условиях.
3. Определить удельную теплоемкость ср смеси кислорода и азота, если количество вещества первого компонента равно 2 моль, а количество вещества второго равно 4 моль.
4. В баллоне находятся аргон и азот. Определить удельную теплоемкость cv смеси этих газов, если массовые доли аргона и азота одинаковы и равны 0,5.
5. Смесь газов состоит из хлора и криптона, взятых при одинаковых условиях и в равных объемах. Определить удельную теплоемкость ср смеси.
Задача 2
1. Найти показатель адиабаты для смеси газов, содержащей гелий массой 10 г и водород массой 4 г.
2. Смесь газов состоит из аргона и азота, взятых при одинаковых условиях и в одинаковых объемах. Определить показатель адиабаты у такой смеси.
3. Найти показатель адиабаты у смеси водорода и неона, если массовые доли обоих газов в смеси одинаковы и равны w=0,5.
4. Найти показатель адиабаты у смеси газов, содержащей кислород и аргон, если количества вещества того и другого газа в смеси одинаковы и равны v.
5. Определить показатель адиабаты частично диссоциировавшего газообразного азота, степень диссоциации а которого равна 0,4.
Задача 3
1. Баллон вместимостью V1=20 л содержит водород при температуре Т1=300 К под давлением р1=0,4 МПа. Каковы будут температура Т2 и давление р2 если газу сообщить количество теплоты Q=6 кДж?
2. Кислород при неизменном давлении р=80 кПа нагревается. Его объем увеличивается от V1=1 м3 до V2=3 м3. Определить: 1) изменение ΔU внутренней энергии кислорода; 2) работу A, совершенную им при расширении; 3) количество теплоты Q, сообщенное газу.
3. Азот нагревался при постоянном давлении, причем ему было сообщено количество теплоты Q=21 кДж. Определить работу A, которую совершил при этом газ, и изменение ΔU его внутренней энергии.
4. Кислород массой 2 кг занимает объем 1 м3 и находится под давлением 0,2 МПа. Газ был нагрет сначала при постоянном давлении до объема З м3, а затем при постоянном
объеме до давления 0,5 МПа. Найти: 1) изменение внутренней энергии ΔU газа; 2) совершенную им работу A; 3) количество теплоты Q, переданное газу. Построить график процесса.
5. Гелий массой 1 г был нагрет на ΔT=100 К при постоянном давлении р. Определить: 1) количество теплоты Q, переданное газу; 2) работу A расширения; 3) приращение ΔU внутренней энергии газа.
Задача 4
1. Идеальный двухатомный газ, содержащий количество вещества l моль, совершает цикл, состоящий из двух изохор и двух изобар. Наименьший объем Vmin=10 л, наибольший Vmax= 20 л, наименьшее давление рmin==246 кПа, наибольшее рmaх=410 кПа. Построить график цикла. Определить температуру Т газа для характерных точек цикла и его термический КПД.
2. Идеальный двухатомный газ, содержащий количество вещества v=l моль и находящийся под давлением p1=0,l МПа при температуре T1=300 К, нагревают при постоянном объеме до давления p2=0,2 МПа. После этого газ изотермически расширился
до начального давления и затем изобарно был сжат до начального объема V1. Построить график цикла. Определить температуру T газа для характерных точек цикла и его термический КПД.
3. Одноатомный газ, содержащий количество вещества v=0,1 кмоль, под давлением p1=100 кПа занимал объем V1=5 м3. Газ сжимался изобарно до объема V2=l м3, затем сжимался адиабатно и расширялся при постоянной температуре до начальных объема и давления. Построить график процесса. Найти: 1) температуры T1, Т2, объемы V2, V3 и давление p3, соответствующее характерным точкам цикла; 2) количество теплоты Q1, полученное газом от нагревателя; 3) количество теплоты Q2 переданное газом охладителю; 4) работу A, совершенную газом за весь цикл; 5) термический КПД цикла.
4. Идеальный многоатомный газ совершает цикл, состоящий из двух изохор и двух изобар, причем наибольшее давление газа в два раза больше наименьшего, а наибольший объем в четыре раза больше наименьшего. Определить термический КПД цикла.
5. Определить работу А34 изотермического сжатия газа, совершающего цикл Карно, КПД которого η = 0,4, если работа изотермического расширения равна А12 = 8 Дж.
Задача 5
1. Смешали воду массой m1=5 кг при температуре T1= 280 К с водой массой m2=8 кг при температуре T2=350 К. Найти: 1) температуру T смеси; 2) изменение AS энтропии, происходящее при смешивании.
2. В результате изохорного нагревания водорода массой m=l г давление р газа увеличилось в два раза. Определить изменение ΔS энтропии газа.
3. Найти изменение AS энтропии при изобарном расширении азота массой m=4 г от объема V1=5 л до объема V2=9 л.
4. Кусок льда массой m=200 г, взятый при температуре t1=—10 °С, был нагрет до температуры t2=0 °C и расплавлен, после чего образовавшаяся вода была нагрета до температуры t=10 °С. Определить изменение ΔS энтропии в ходе указанных процессов.
5. Лед массой m1=2 кг при температуре t1=0 °С был превращен в воду той же температуры с помощью пара, имеющего температуру t2= 100 °С. Определить массу m2 израсходованного пара. Каково изменение ΔS энтропии системы лед—пар?
Задача 6
Найти закон распределения температуры Т(x,t) в стержне конечной длины L, для которого задано распределение температуры в начальный момент времени T(x,0) и на концах стержня поддерживается постоянная температура.
1.
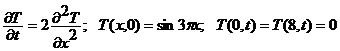
2.

3.
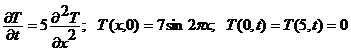
4.
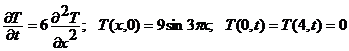
5.
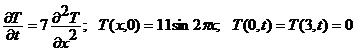
Задача 7
Найти закон распределения температуры Т(x,t) в стержне конечной длины L, для которого задано распределение температуры в начальный момент времени T(x,0) и концы которого теплоизолированы.
1.

2.

3.

4.
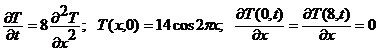
5.
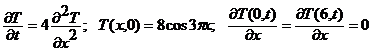
Автор страницы: admin




